Unser Produktionsstandort
Tierkomponentenfreie Herstellung von Trockenpulver und flüssigen Produkten.
Mit unserem neuen Produktionsstandort in der Nähe von Bielefeld, erschließen wir neue Dimensionen für unsere internen Produktionskapazitäten, auf der Grundlage eines nach ISO 9001 und ISO 13485 zertifizierten Qualitätsmanagementsystems. Unsere hoch moderne Einrichtung, die frei von Materialien tierischen Ursprungs ist, ermöglicht die flexible Herstellung von Pulvern und flüssigen Produkten sowie die Verflüssigung von Pulvern in kleinem bis großen Maßstab. Unsere erfahrenen Mitarbeiter arbeiten mit modernsten Geräten. Dies macht uns zu einem idealen Partner, der während Ihres gesamten Projekts Auftragsfertigungskapazitäten bereitstellen kann, von Pilotproduktionen bis hin zur Routineanwendung.
Portfolio
Unser Herstellungsspektrum beinhaltet:
- Zellkultur Medien
- Zellkultur Feeds
- Zellkultur Supplemente
- Puffer
- Medizin Produkte
- Nahrungsergänzungsmittel
- Analytische Standards
- und vieles mehr, nicht nur für Produkte von Xell, sondern auch für Ihre individuellen Formulierungen
Xell hat sich zu Agilität und Flexibilität verpflichtet, ohne dabei Qualität, Vorlaufzeit und Reaktionszeiten zu vernachlässigen
Unser Produktionsstandort bietet:
- Produktion zu 100% frei von tierischen Komponenten
- Flexibilität für Chargen- und Abpackungsgrößen
- Kundenspezifische Anpassungen um deine Projektanforderungen zu erfüllen
- Skalierbarkeit vom Prototyp 1 L/kg/Charge bis 1.000 L/kg/Charge
Unser Team
- Unsere Produktingenieure leiten Sie an, um Ihre Ideen in leistungsfähige Produkte umzusetzen
- Unser Fertigungsteam sorgt für zuverlässige Lieferzeiten
- Unser Analytikteam überprüft kontinuierlich die Materialkonformität
- Unser Qualitätsteam unterstützt Sie mit der erforderlichen Dokumentation, um Ihre Projektanforderungen zu erfüllen
- Unser Kundendienstteam steht Ihnen zur Verfügung , um Sie direkt mit den Experten zu verbinden
- State-of-the-art Pulverproduktion
- Stahlstiftmühle (Deutschland)
- Inertgas und temperaturkontrolliert
- Flexible Flüssigproduktion
- Qualifiziertes Membran WFI System (Deutschland)
- Hoch flexible Abfüllung
- WFI (Wasser für Injektionszwecke)
- SSL Tanks (Größe: 50 L to 1.000 L)
- Reinräume der ISO Klasse 8 – 5
- Kühlraum zur Lagerung von Palettenware
- Entwickelt für modulare Erweiterung
- DIN EN ISO 9001 und DIN EN ISO 13485 konformes QMS
- Abgenommen durch regelmäßige Audits von Kunden aus der Biotechnologie- und Biopharmaindustrie
Pulverprodukte
- 1 bis 300 kg/Charge (≈ 9.000 L Medium)
- Bis zu 1.000 kg/Charge (≈ 40k L Medium) – Etablierung erfolgt in 2022
- Derzeitige jährliche Produktionskapazität: 30,000 kg – in 2022: 140,000 kg/Jahr
Flüssigprodukte
- Bis zu 1.000 L/Charge (Edelstahl Tanks)
- Bis zu 8.000 L/Charge – Etablierung erfolgt 2023
- Flexible Abfüllung in Flaschen (0,01 L bis 1 L) oder Bags (5 L bis 500 L)
- Derzeitige jährliche Produktionskapazität: 220,000 L
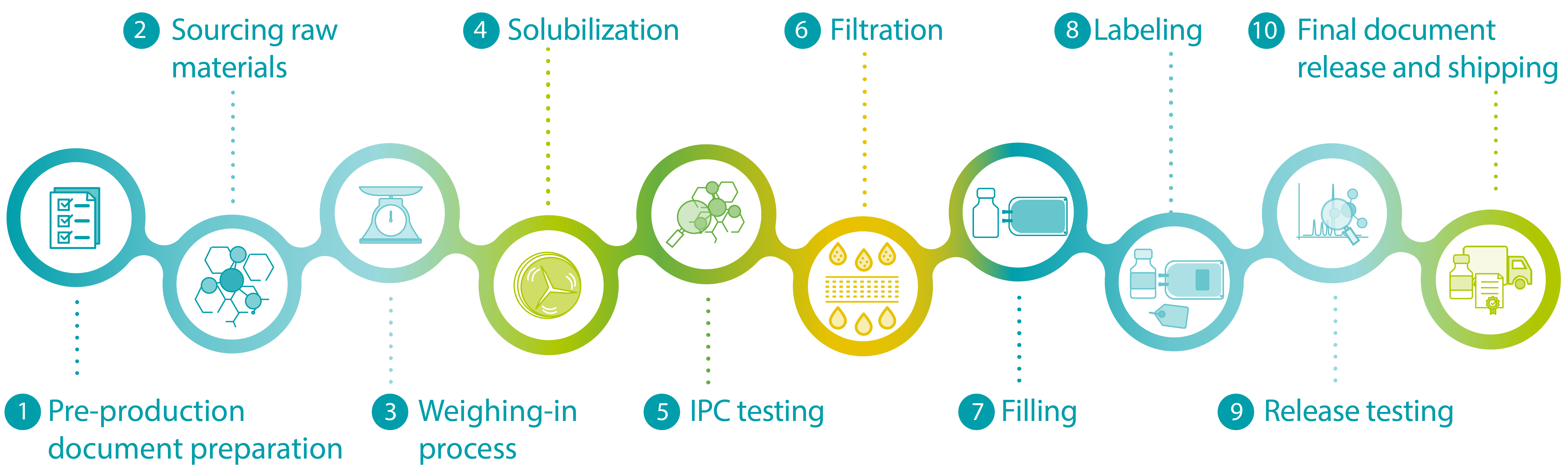
Abbildung:Überblick über Xells Produktionsprozess für Flüssigmedien.
Unser standardisiertes Pulverherstellungsverfahren kann an spezifische Formulierungen angepasst werden (z.B. für Puffer oder basale Zellkultur Medien), um final ein qualitativ hochwertiges Pulver zu erhalten. Zusätzlich zu intern festgelegten Prozessen können kundenspezifische Anforderungen integriert werden, einschließlich Rohstoffbeschaffung, zusätzliche erforderliche Dokumente, weitere analytische Spezifikationen für die finale Freigabe sowie die Produktverpackung.
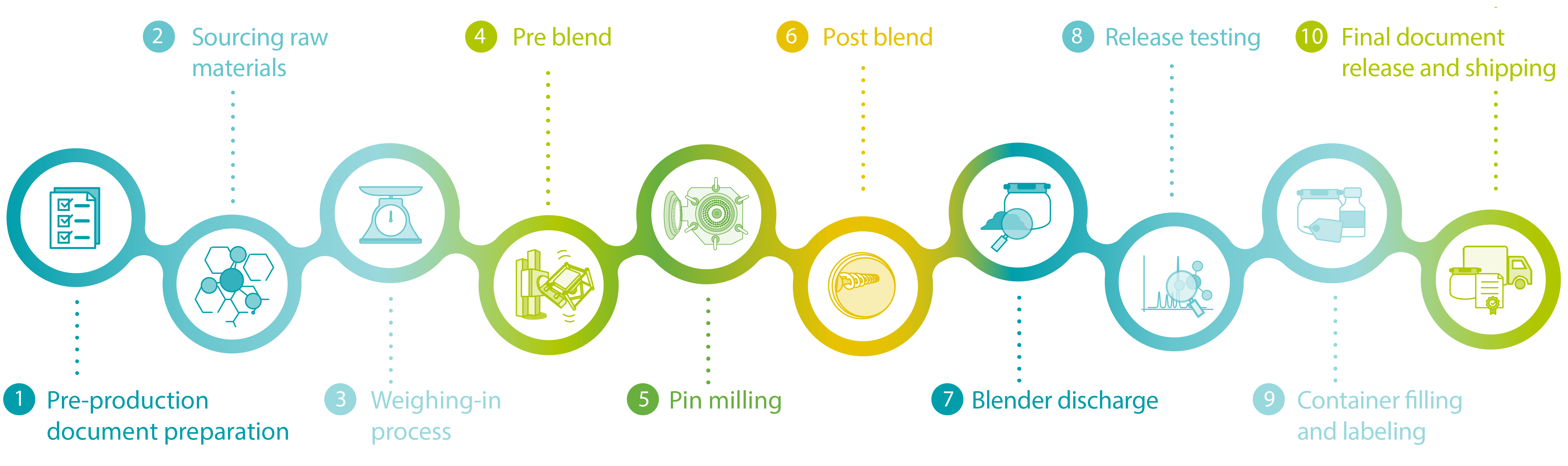
Unser Produktionsprozess lässt sich wie folgt zusammenfassen:
1. Vorbereitung der Dokumente
Produktspezifische Dokumente umfassen: Produktspezifikationen, spezifische Etikettenvorlagen, Produktionsprotokoll (MBR), spezifische Abfüllung in entsprechende Behältnisse, Sicherheitsdatenblätter, Zertifikatvorlagen usw.
2. Beschaffung von Rohstoffen
Die Auswahl erfolgt nach internen Standardspezifikationen oder kundenspezifischen Anforderungen. Ein hoher Rohstoffstandard für Zellkulturmedien wird vorausgesetzt.
3. Wägevorgang
Erfolgt gemäß der produktspezifischen Formulierung innerhalb einer ISO-Klasse 5-Umgebung. Auf Kundenwunsch können unsere Produktingenieure bei der Optimierung eines solchen Verfahrens für kundeneigene Formulierungen behilflich sein.
4. Vormischen
Die gesamte Formulierung wird vorvermischt. Abhängig vom Konzentrationsverhältnis in der Endformulierung können auch einzelne Rohstoffe für eine optimale Verteilung/Homogenität vorvermahlen werden.
5. Vermahlung in der Stiftmühle
Der Mahlprozess ist produktschonend und findet unter temperaturgesteuerten Inertgasbedingungen statt.
6. Nachvermischung
Während und nach dem Mahlprozess findet ein zusätzliches Mischen statt, um eine homogene Rohstoffverteilung im finalen Pulverprodukt zu erreichen.
7. Entnahme aus dem Mischer
Das Pulver wird zunächst in loser Schüttung abgefüllt, hierbei werden zusätzliche Proben zur Testung der Produktlöslichkeit und der analytischen Datenerfassung für die Produktfreigabe entnommen.
8. Produktfreigabe
Die Standardfreigabemessungen sind in der Sektion XXX aufgeführt und können spezifisch erweitert werden.
9. Abfüllung und Etikettierung
Nach der Chargen-Freigabe des Produkts gemäß der definierten Materialspezifikation erfolgt die produkt- oder kundenspezifische Abfüllung und Kennzeichnung.
10. Finale Freigabe und Versand
Die finale Dokumentfreigabe enthält das chargenspezifische CoC oder CoA, etablierte Verflüssigungsprotokolle etc.
Flüssig- und Pulver-Medien: Unterschiede und Vorteile
Flüssige Zellkulturmedien, Supplemente, Puffer und ähnliche Produkte sind die bevorzugte Wahl für Tests im kleinen Maßstab und wenn Zeit ein entscheidender Faktor ist. Sie sind als gebrauchsfertige Produkte konzipiert und sparen Zeit und Ressourcen, die andernfalls zum Lösen von Pulvern und weiteren Schritten benötigt werden. Darüber hinaus können flüssige Produkte nach dem Öffnen der Flaschen für einen gewissen Zeitraum verwendet werden (bei einer Handhabung gemäß der Produktanforderungen sowie der sterilen und guten Laborpraxis). Dies macht flüssige Produkte zur idealen Wahl, sollten über einen bestimmten Zeitraum kleinere Mengen benötigt werden.
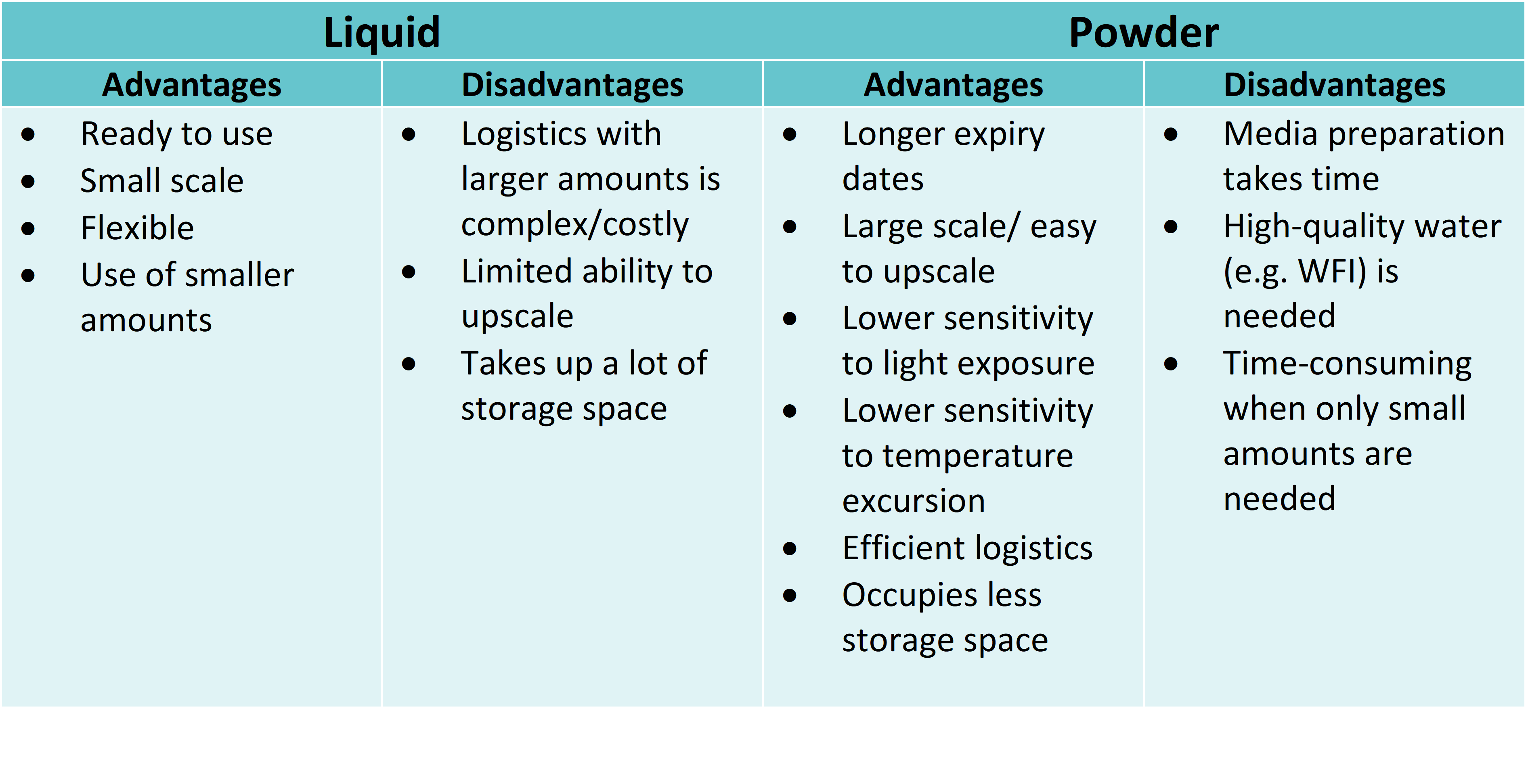
Pulverförmige Medien, Supplemente und Puffer werden im Allgemeinen für Großproduktionen empfohlen. Dies hat mehrere Gründe, darunter ein längeres Haltbarkeitsdatum (im Vergleich zu Flüssigprodukten), eine geringere Empfindlichkeit gegenüber Lichtexposition (aufgrund der Verpackung in HDPE-Behältern) und bequemere Verpackungsgrößen (~ 25 kg Trockenpulver entsprechen 1000 L flüssigem Medium). Last but not least sind die Transport- und Lagerkosten im Vergleich zu flüssigen Produkten wesentlich niedriger.
Tabelle. 1: Vorteile und Nachteile von Flüssig- und Pulver-Medien.
CMO Services
- Prototyping im kleinen Maßstab mit hoher Flexibilität
- Unterstützung und Implementierung Ihres Scale Ups
- Routinemäßige Belieferung mit Flüssig- und Pulverprodukten
CRO Services
- Rohstoffprüfungen (z. B. Chargen Konsistenz)
- Bewertung von Rohstofflieferanten (Unterstützung bei change control und impact analysis)
- Formulierungsprüfung
Qualität
Das Qualitätsmanagementsystem von Xell entspricht der DIN EN ISO 9001 und der DIN EN ISO 13485, wird jährlich überprüft und von einer externen, unabhängigen Stelle zertifiziert.
Maßnahmen zur Archivierung und Rückverfolgbarkeit von Chargenprotokollen gewährleisten eine solide Grundlage für Untersuchungen oder regulatorische Belange. Etablierte Prozesse zur Messung der Produkt- und Servicequalität sowie wissenschaftliche Ursachenanalysen in Kombination mit einem geeigneten CAPA-Verfahren ermöglichen unsere Lieferanten und uns eine kontinuierliche Verbesserung.
Möchten Sie weitere Informationen erhalten, mehr über das Qualitätsmanagementsystem von Xell und die Anwendung unserer Produkte und Dienstleistungen für die GMP-Fertigung in Erfahrung bringen, oder ein Remote- bzw. Vor-Ort-Audit durchführen? Dann kontaktieren Sie uns.
Auswahl der Rohmaterialien
- Die Qualitätsklassifizierung wird für allein der Produktion genutzten Rohstoffe durchgeführt
- Die wichtigsten Faktoren für uns sind die Spezifikation und Qualität (USP, EP, JP) des jeweiligen Rohmaterials sowie die Rückverfolgbarkeit/Dokumentation des Materials und des Lieferanten
- Die Vergleichbarkeit verschiedener Chargen wird überwacht
- Ein zweiter Rohstofflieferant ist etabliert (Supply Chain Security)
Prüfung der eingehenden Rohstoffe
- Identitätsprüfung für Rohstoffe mittels FTIR (falls zutreffend)
- Bioburden-Quantifizierung für definierte/kritische Rohstoffe
- Eine Feuchtigkeitsmessung wird für definierte/klassifizierte Komponenten durchgeführt
- Die Überprüfung der Chargendokumentation (z. B. CoA, CoO und CoP) ist ein obligatorischer Bestandteil unseres Verfahrens zur Freigabe von Rohstoffen
- Ablaufdaten oder Nachprüfungen dieser Daten werden überwacht bzw. durchgeführt – Studien zur Haltbarkeitsprüfung laufen kontinuierlich
Case Study:Rohstoffkontrolle – Spurenelementkontaminationen von Aminosäuren
Aminosäuren sind ein Hauptbestandteil von Zellkulturmedien, die auch einen signifikanten Prozentsatz der Medien- und Feed Supplement-Zusammensetzung ausmachen. In unserer Technotezeigen wir, dass Rohstoffe für Aminosäuren von verschiedenen Lieferanten unterschiedliche Spurenelementverunreinigungen aufweisen.
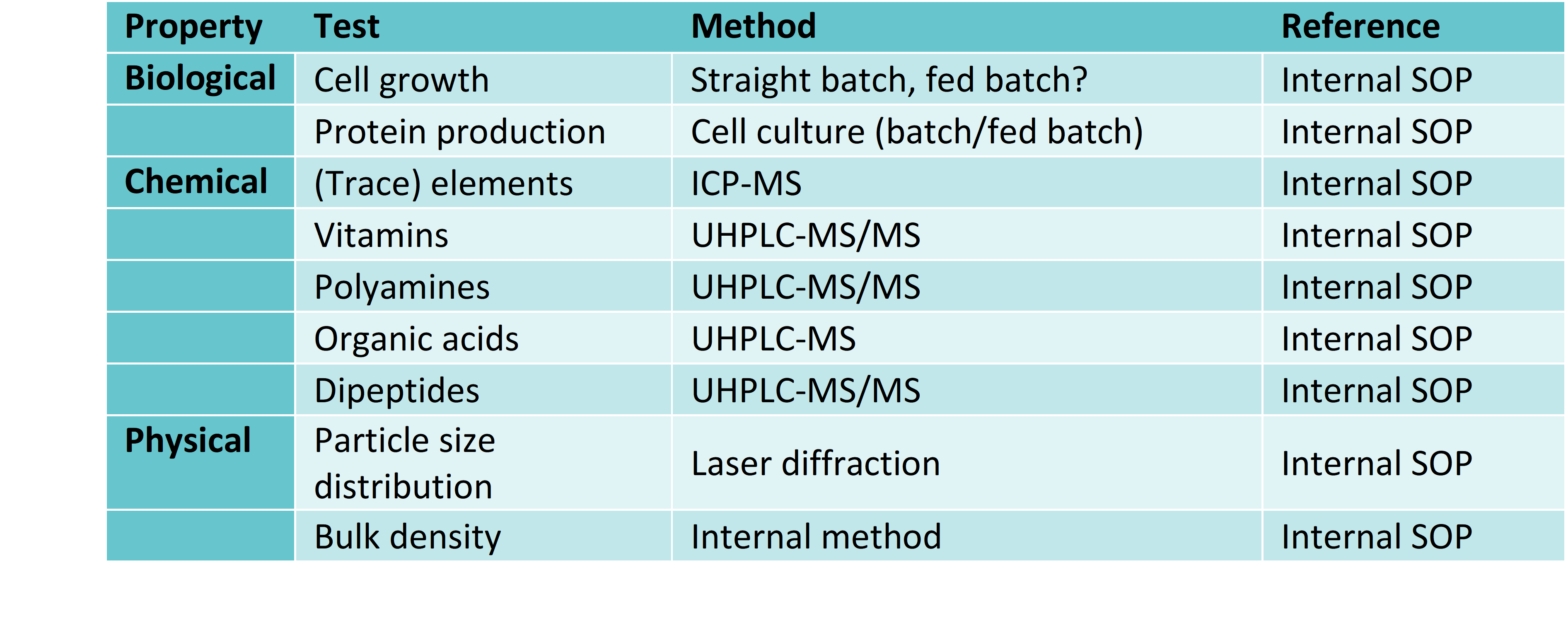
Unsere Standardtests
Vor der Freigabe durch das Qualitätsmanagement werden die biologischen, chemischen und physikalischen Qualitätsmerkmale einer Charge gemäß der jeweiligen Richtlinien überprüft. Die biologischen Tests zeigen die Gesamtqualität des Produktionsprozesses und der Produkthandhabung. Die Testergebnisse aus den chemischen und physikalischen Analysen werden hauptsächlich durch die Produktformulierungs- und Herstellungsschritte, wie der Verflüssigung (für flüssige Produkte) oder den Misch- und Mahlvorgänge (für trocken pulverförmige Produkte) beeinflusst.
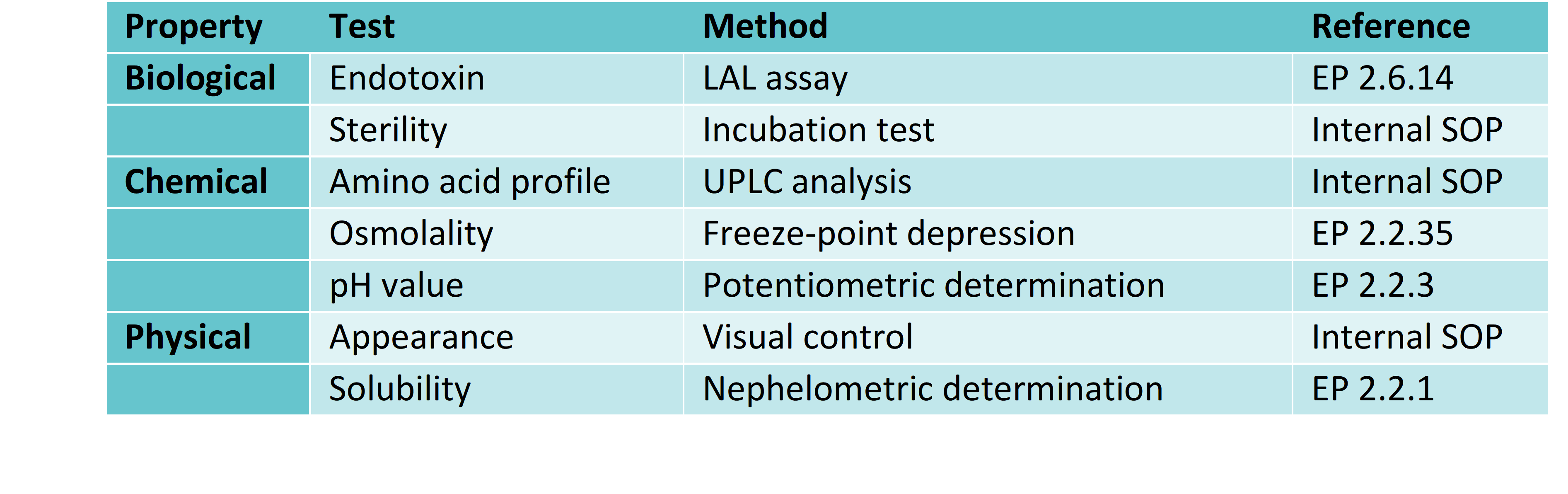
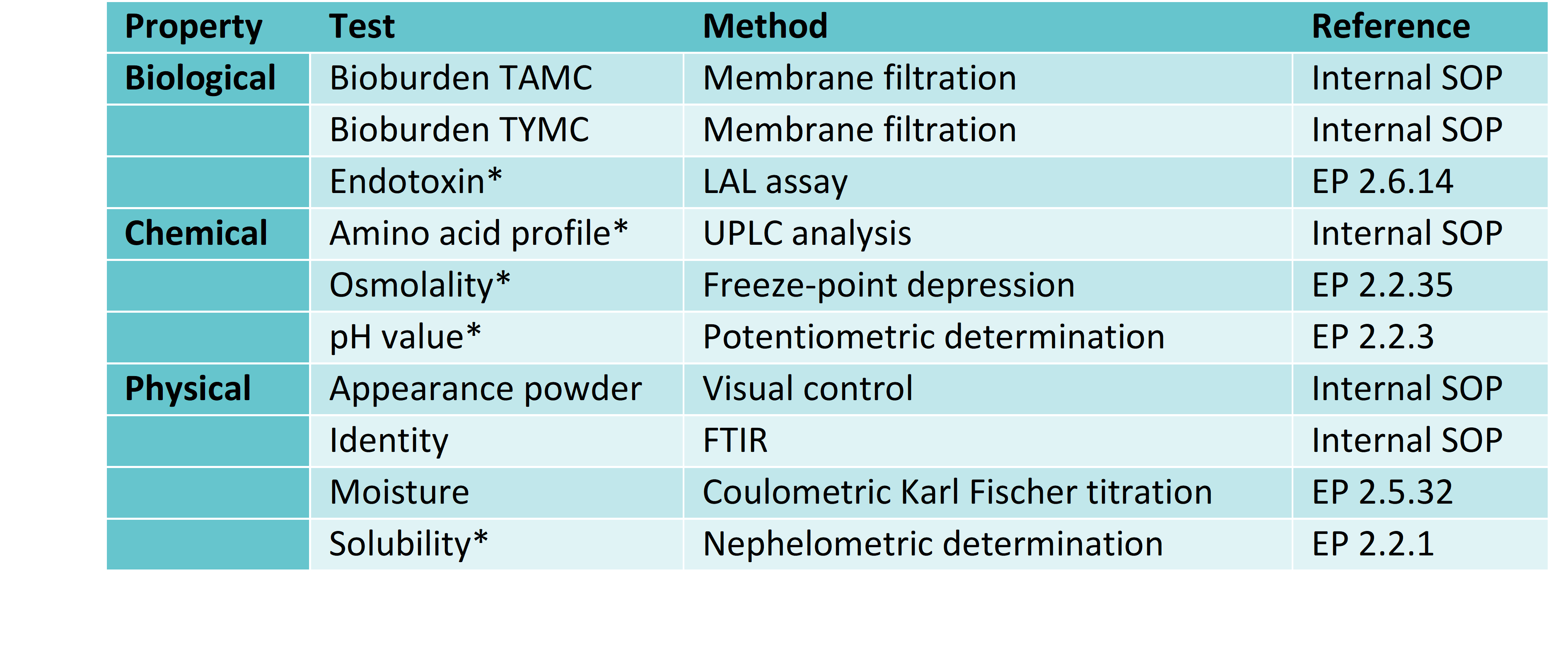
Jede Charge unser Flüssig- und Pulver-Medien sowie unserer Supplemente muss den definierten, produktspezifischen Parametern der in den Tabellen 1 und 2 aufgeführten Qualitätsmerkmale entsprechen.
Tabelle 1: Übersicht über die standardmäßig durchgeführten analytischen Tests bei Flüssigmedien.
Tabelle 2: Übersicht über die standardmäßig durchgeführten analytischen Tests bei Pulvermedien. *entsprechend des Lösungsprotokolls.
Erweitertes Testpanel
Benötigen Sie mehr Testdaten als unser Standardpanel hergibt? Gerne bewerten oder implementieren wir weitere Tests zur Materialfreigabe oder zu Ihrer Information.
Wenn Sie einen Parameter vermissen, kontaktieren Sie uns gerne, wir sind immer offen für die Entwicklung kundenspezifischer Analysemethoden.
Tabelle 3: Übersicht über zusätzlich verfügbare Tests für Xell Produkte oder weite Proben.Besuchen Sie unseren Webshop für zusätzliche Informationen bezüglich unserer analytischen Dienstleistungen.
Zertifikate und Dokumente
Alle unsere Produkte werden mit den folgenden zugehörigen Zertifikaten und Dokumenten geliefert:
- Produktspezifische Dokumente beinhalten:
- Sicherheitsdatenblätter (Material safety data sheets – MSDS)
- Protokolle (Protocols for use – PFUs)
- Herkunftszertifikate
- Lösungsprotokolle
- Chargenspezifische Dokumente beinhalten:
- Analysezertifikate für Flüssig- und Pulver-Medien (Certificates of compliance/analysis – CoC/CoA)
Alle Dokumente können in unserem Webshop im BereichDokumentensuche gefunden und heruntergeladen werden.
Hier sehen Sie unseren einfachen Ansatz zur Hochskalierung eines Prozesses für die AAV8-Produktion in HEK 293-Zellen, die in unserem chemisch definierten, tier- und proteinfreienHEK ViP NX Mediumkultiviert wurden.
Beginnend mit Schüttelkolbenversuchen haben wir unser einfaches, nicht optimiertes Suspensionskulturprotokoll angewendet und erfolgreich in den kontrollierte Bioreaktor-Maßstab übertragen, was zu erhöhten AAV8-Genomtitern führte. Dies ist nur ein weiterer Nachweis, der die Wirksamkeit unserer HEK ViP-Produktreihe belegt.
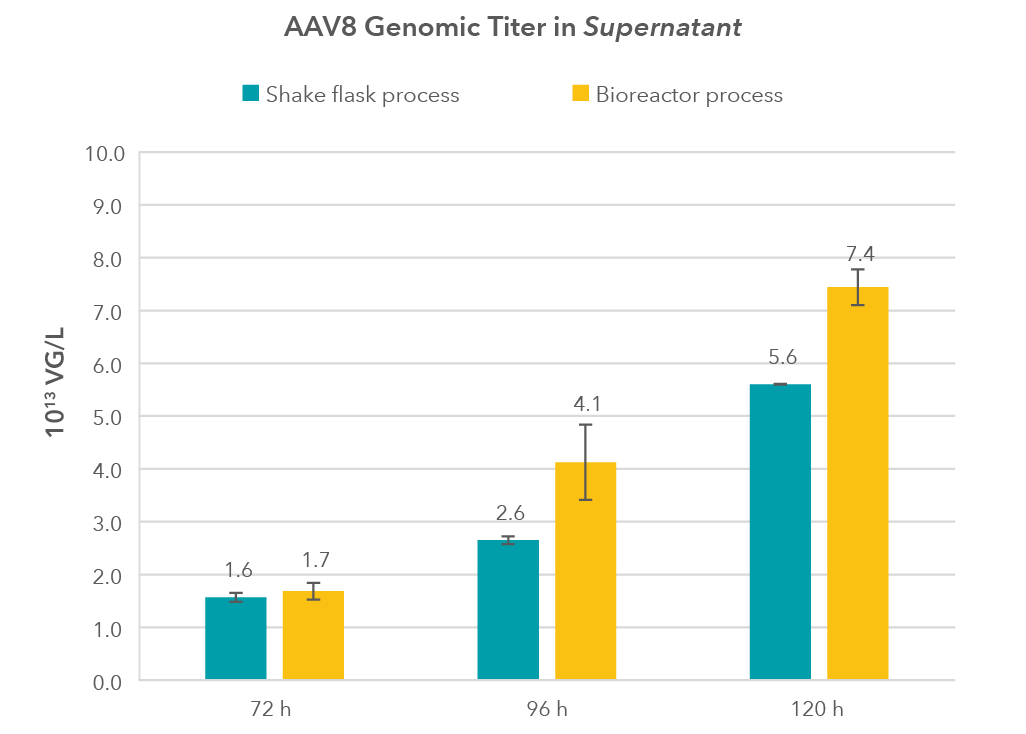
Abbildung 1: Vergleich von genomischen AAV8 Titern in Zellkulturüberständen von HEK293 Zellen in Xell’s HEK ViP NX Medium. Eine Kultivierung im Bioreaktor führt zu einer erhöhung der genomischen Titer im Zellkulturübertand
Unser chemisch definiertesHEK Feed Supplement unterstützt die Produktion von rekombinanten Proteinen und Antikörpern in Suspensioskulturen durch Aufrechterhaltung und Verlängerung der Produktionskapazität von HEK-Kulturen. Verbrauchte Substanzen, wie Vitamine und Aminosäuren, werden aufgefüllt, um die Proteinausbeute durch Prozessverlängerung zu erhöhen.
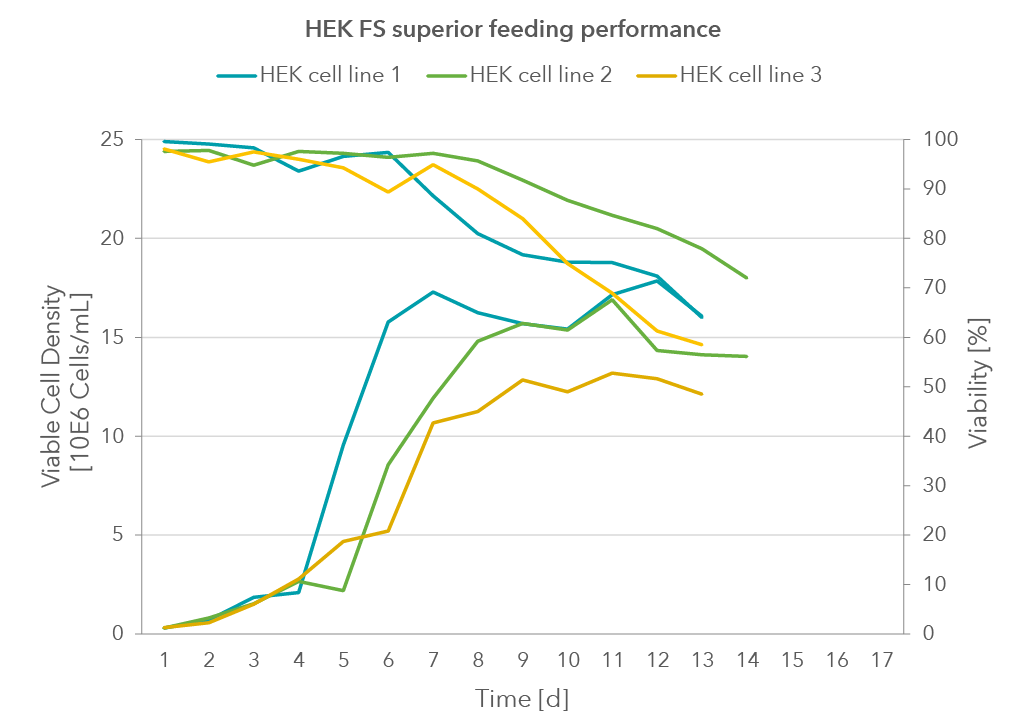
Abbildung 2:Viable Zelldichte (VCD) und Viability von verschiedenen HEK Zelllinien in einem Fed-batch Prozess. Mit Xell’s HEK FS Feed Supplement konnten verbrauchte Substanzen wieder aufgefüllt und so die Produktionsfähigkeit verbessert werden.
Unser chemisch definiertesCHOlean Medium wurde mit einem minimalen Set aus gut ausgewogenen Komponenten entwickelt, um eine schlanke, robuste und flexible Mediumbasis zu erhalten. Darüber hinaus ist es in der Lage, mit state-of-the-art Medien um das höchste Zellwachstum und den höchsten Produkttiter zu konkurrieren. Die Formulierung ist für ein breites Spektrum verschiedener CHO-Zelllinien geeignet, einschließlich K1 und DG44. Zudem ist CHOlean für die einfache Adaption aus anderen Medien optimiert und ist Ihre robuste Plattform, um leistungsstarke Fed-Batch-Prozesse darauf aufzubauen.
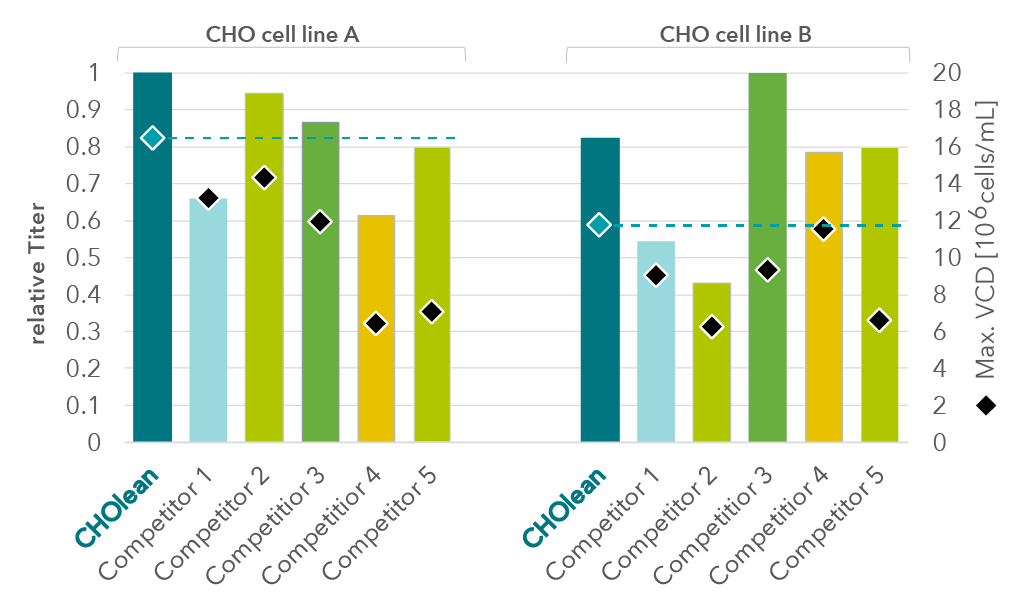
Abbildung 3: Relative Titer (Säulen) und maximale viable Zelldichten (VCD, Rauten) von zwei CHO Zelllinien in CHOlean im Vergleich zu state-of-the-art, CD, ADCF Expressionsmedien für CHO Suspensionszellen von fünf verschiedenen Wettbewerbern. Zum Vergleich wird der Bereich der üblichen viablen Zelldichten für CHO-Zelllinien in einer Basalmediumformulierung, z. DMEM / Ham’s F12.
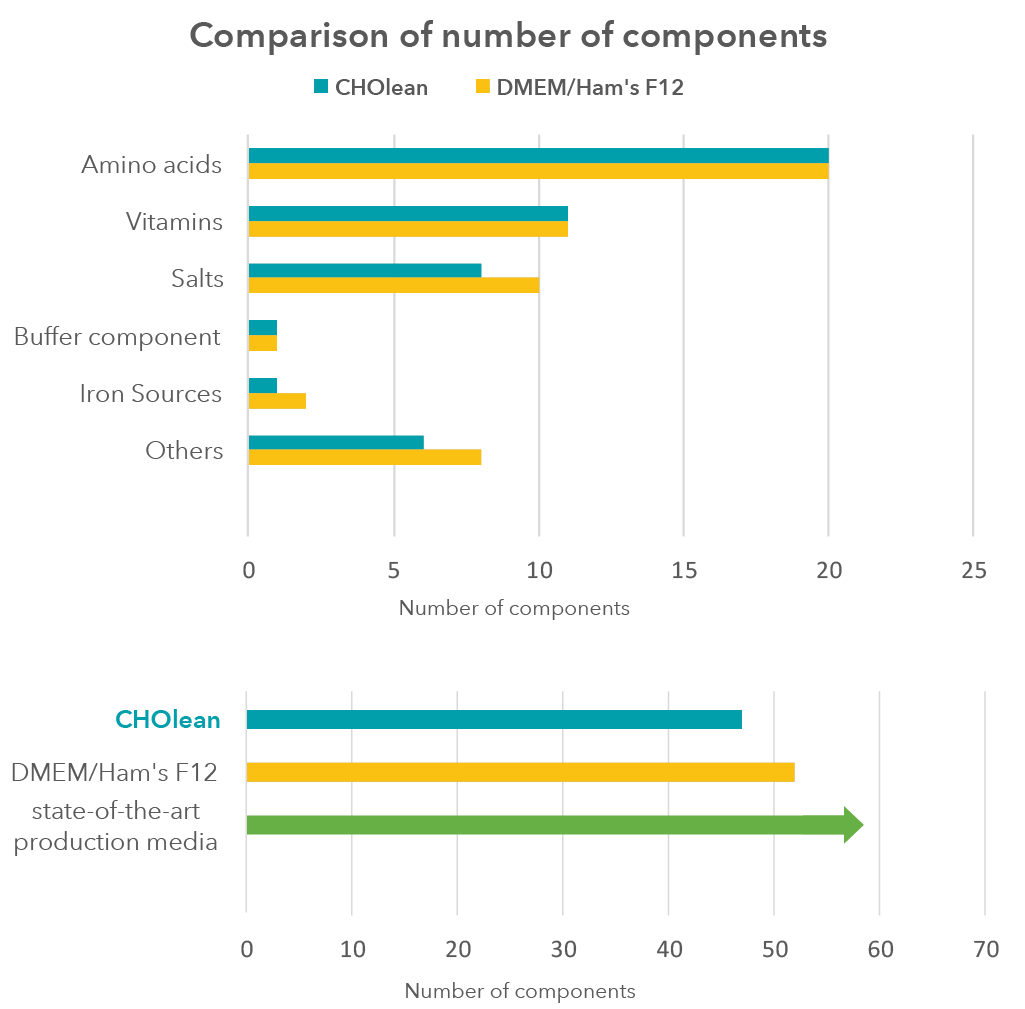
Abbildung 4: Anzahl von Komponenten verschiedener Klassen (Aminosäuren, Vitamine, Salze, Puffer, Eisen und weitere) vonCHOlean im Vergleich zu der basalen Formulierung von DMEM/Ham’s F12, sowie der Vergleich der Gesamtzahl an Komponenten von CHOlean, DMEM/Ham’s F12 und einigen state-of-the-art Produktionsmedien.
Verpackung und Logistik
Uns ist bewusst, dass ein effektiver Versand-, Liefer- und Lagerungsprozess genauso wichtig ist wie der Produktionsprozess an sich. Aus diesem Grund ist es für uns von größter Bedeutung, unsere Produkte bestmöglich zu Verpacken und eine schnelle Lieferung unter Berücksichtigung der Produkt- und Kundenbedürfnisse zu ermöglichen. Abhängig von der Menge, Größe und Empfindlichkeit des Produkts haben wir eine Reihe von Verpackungs- und Versandoptionen geschaffen, um alle Anforderungen zu erfüllen und unsere hohen Standards auch während des gesamten Versandprozesses aufrechtzuerhalten.
Nach der Produktion werden unsere Produkte in einem temperaturüberwachten (+ 2-8 ° C) Kühlhaus gelagert bis sie versandbereit sind.
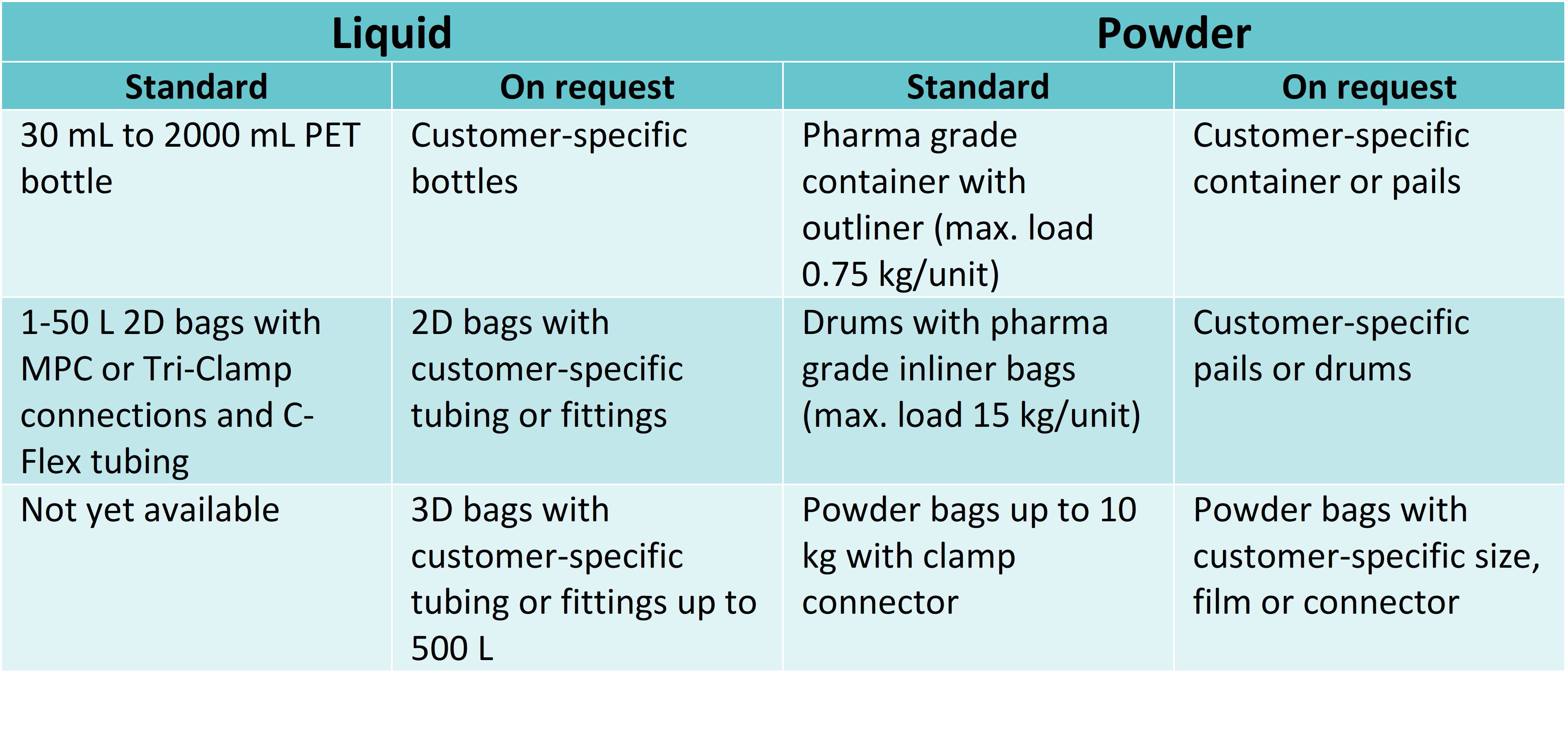
Wir bieten derzeit bereits verschiedene Verpackungsoptionen und -größen für unsere Produkte an. Gerne implementieren wir jedoch noch weitere Optionen, um kundenspezifische Anforderungen zu erfüllen (s. Tabelle 1). Bitte besprechen Sie Ihre Ideen mit uns.
Tabelle. 1:Optionen für die Verpackung von Flüssig- und Pulvermedien.
Wir liefern global – egal wo auf der Welt Sie sich befinden Wenn Sie unsere Medien oder Dienstleistungen benötigen, werden wir einen Weg finden, Sie gemeinsam mit unseren etablierten Logistikpartnern zu beliefern. Wir reagieren flexibel auf Ihre Anforderungen in Bezug auf Verpackung, Transportüberwachung und Transportorganisation.
Zudem arbeiten wir nur mit ausgewählten Vertragspartnern zusammen, die garantieren können, dass die spezifischen Anforderungen unserer Produkte erfüllt werden. Wir versenden grundsätzlich per Express, um lange Wartezeiten und Leerlaufzeiten so weit wie möglich zu vermeiden und können auf Wunsch auch eine Temperaturüberwachung mittels Temperaturerfassungssystemen und Lieferverfolgung anbieten.
In Bezug auf die Verpackung stehen verschiedene Optionen zur Verfügung, wie z. B. passive Kühlung, kontinuierliche Kühlung, temperaturgesteuerter Versand usw. Im Allgemeinen versenden wir kleinere Mengen flüssiger Medien per Express ohne Kühlung (Lieferung innerhalb von 24 bis 48 Stunden). Pulvermedien oder größere Mengen an Flüssigkeiten werden grundsätzlich in gekühlten Styroporboxen/oder -Paletten geliefert. Größere Mengen werden passiv gekühlt auf Paletten verschickt.
Je nach Bestimmungsort und Warenmenge verwenden wir:
- Europaletten
- Styroporboxen
- Thermoshipper
- Aktiv gekühlte Kontainer
- …
Wenn Sie spezielle Anforderungen bezüglich des Transports oder der Verpackung haben, zögern Sie bitte nicht, uns zu kontaktieren, um die verfügbaren Optionen zu besprechen.